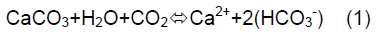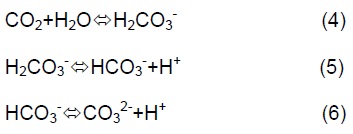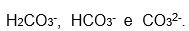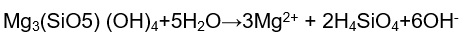ACQUE BICARBONATO-CALCICHE E BICARBONATO-CALCICHE MAGNESIACHE
|
Si definiscono bicarbonato-calciche quelle acque che presentano una prevalenza netta del contenuto in ione bicarbonato e ione calcico rispetto alla quantità totale degli altri ioni principali.
Vengono definite bicarbonato-calciche-magnesiache quelle acque che hanno un contenuto di ione magnesio relativamente abbondante rispetto allo ione calcio. I processi chimici in grado di generare queste acque sono generalmente legati alla dissoluzione dei carbonati, operata dalle acque meteoriche.(1). Questa reazione è fortemente influenzata dalla temperatura, dalla pressione parziale di CO2 e dal PH.
L’anidride carbonica dell’atmosfera reagisce con l’acqua per formare acido carbonico (H2CO3-) secondo la reazione 4 essendo un acido debole si ionizza per gradi (5,6). La CO2 può avere diverse origini: Atmosferica, vulcanica, può derivare dalla decomposizione, dissoluzione CaCO3, dalla precipitazione della calcite per la reazione del gesso con HCO3-, può risalire da fratture profonde ed avere un’origine Mantellica.
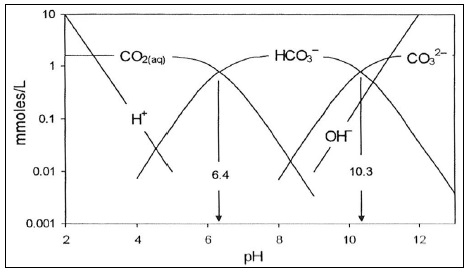
Fig. : Frazione molare delle specie H2CO3,HCO3-e CO32-in acqua pura a 24°Cin funzione del PH(da Fornaseri, 1998, ridisegnato).
La CO2 che si scoglie nelle acque determina la presenza contemporanea di :
Quale di queste specie sarà predominate in soluzione acquosa dipenderà dal PH della soluzione.
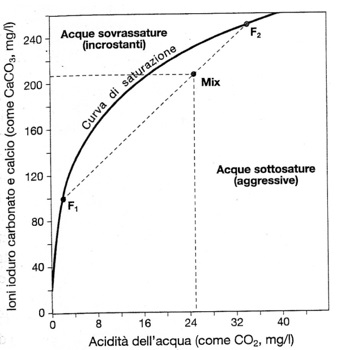
I carbonati di origine dissolutiva possono essere legati a rocce coerenti o semicoerenti (calcari, dolomie, travertini, marmi, marne, calacreniti, arenarie silicee a cemento carbonatico, conglomerati e brecce carbonatiche o silicee a cemento carbonatico) oppure sciolte (sabbie e ghiaie di natura carbonatica). Anche il carbonato di calcio precipitato nelle fratture di rocce coerenti o nei pori delle rocce sciolte, in condizioni climatiche diverse da quelle attuali può contribuire alla genesi di acque di facies bicarbonatiche Nei sistemi carsici le acque bicarbonatiche possono essere aggressive (sottosature rispetto al CaCO3) e sciogliere il calcare, o incrostanti (sovrassature) e depositare il calcare. Il diagramma di Tillmans rappresenta graficamente i concetti di saturazione, sovrassaturazione e sottosaturazione. Fig. : Diagramma di Tillmans
La saturazione è espressa in funzione del contenuto in CaCO3 (mineralizzazione dell’acqua) e dalla sua acidità naturale, fornita dalla CO2.
Questo diagramma vale solo per le acque dove tutto il carico minerario è dato dalla messa in soluzione del calcare e in assenza di piogge acide legate a emissioni antropiche di gas. La curva di saturazione separa le acque aggressive (sottosature) da quelle incrostanti (sovrassature), il mescolamento di due acque in equilibrio con mineralizzazione quantitativamente molto diversa (F1-F2), genera un acqua aggressiva (Mix). Nelle acque circolanti in rocce dolomitiche CaMg(CO3)2, nonostante la bassa solubilità, c’è un arricchimento dello ione Mg2+. Quando però il tenore di Mg2+ supera quello del calcio, l’origine del magnesio Questo arricchimento può essere dato dall’idrolisi di rocce cristalline femiche come ad esempio il serpentino: |