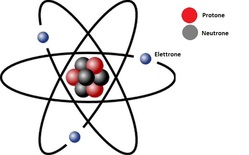
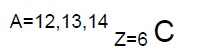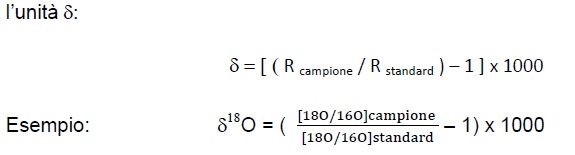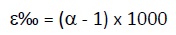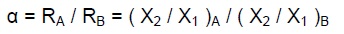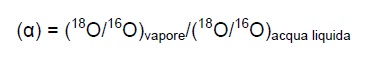In ogni Atomo indipendentemente dall’ elemento a cui appartiene, la carica positiva di protoni del nucleo e le cariche negative degli elettroni si bilanciano sempre. Il numero di elettroni o di protoni, differenziano ogni elemento dagli altri e ne determina il comportamento chimico.
Il neutrone non ha carica ed è leggermente più pesante di un protone, essi hanno il compito di neutralizzare la repulsione elettrica tra i protoni ammassati nel nucleo.
Ogni elemento si distingue per il numero di protoni contenuti nel nucleo atomico ma il numero di neutroni all’ interno di esso può variare. Di quasi tutti gli elementi, esistono in natura forme secondarie che si differenziano da quelle principali per il numero di neutroni. Questi atomi si chiamano isotopi dal greco isos (uguale) e topos (luogo): essi infatti occupano la medesima posizione nella tavola periodica, avendo lo stesso numero di protoni. Uno stesso elemento può presentare una varietà di nuclei diversi che si differenziano per il numero di neutroni.
Il numero atomico (Z) indica il numero di protoni (e quindi degli elettroni) presenti in un atomo. La somma dei protoni e dei neutroni si definisce invece numero di massa (A). Gli isotopi sono quegli atomi che, a parità di Z, hanno diverse masse atomiche A
Per esempio il carbonio avrà:
Il neutrone non ha carica ed è leggermente più pesante di un protone, essi hanno il compito di neutralizzare la repulsione elettrica tra i protoni ammassati nel nucleo.
Ogni elemento si distingue per il numero di protoni contenuti nel nucleo atomico ma il numero di neutroni all’ interno di esso può variare. Di quasi tutti gli elementi, esistono in natura forme secondarie che si differenziano da quelle principali per il numero di neutroni. Questi atomi si chiamano isotopi dal greco isos (uguale) e topos (luogo): essi infatti occupano la medesima posizione nella tavola periodica, avendo lo stesso numero di protoni. Uno stesso elemento può presentare una varietà di nuclei diversi che si differenziano per il numero di neutroni.
Il numero atomico (Z) indica il numero di protoni (e quindi degli elettroni) presenti in un atomo. La somma dei protoni e dei neutroni si definisce invece numero di massa (A). Gli isotopi sono quegli atomi che, a parità di Z, hanno diverse masse atomiche A
Per esempio il carbonio avrà:
Quanti più protoni ci sono in un nucleo atomico, tanto maggiore è il numero di neutroni necessario per contrastare le forze di repulsione che agiscono tra i protoni dicarica positiva. Con il crescere delle dimensioni del nucleo, le forze di repulsione tra i protoni diventano sempre più potenti di conseguenza sarà necessario un numero maggiore di neutroni.
Gli isotopi si dividono in stabili che non cambiano nel tempo (circa 300) e radioattivi (circa 1200) che nel tempo cambiano di peso ma esistono anche isotopi “quasi stabili”.
La loro stabilità è dovuta al fatto che, pur essendo radioattivi, hanno un tempo di dimezzamento estremamente lungo anche se confrontato con l’età della Terra.
La geochimica isotopica si dedica alla determinazione quantitativa dei rapporti di abbondanza dei diversi isotopi di un elemento, le quantità relative di ciascun isotopo, espresse abitualmente in %, rappresentano le abbondanze isotopiche.
Gli isotopi che hanno una certa importanza negli studi idrogeologici sono:
Idrogeno 1H (idrogeno H;
2H (deuterio-D);
3H(Trizio-T)
Gli isotopi si dividono in stabili che non cambiano nel tempo (circa 300) e radioattivi (circa 1200) che nel tempo cambiano di peso ma esistono anche isotopi “quasi stabili”.
La loro stabilità è dovuta al fatto che, pur essendo radioattivi, hanno un tempo di dimezzamento estremamente lungo anche se confrontato con l’età della Terra.
La geochimica isotopica si dedica alla determinazione quantitativa dei rapporti di abbondanza dei diversi isotopi di un elemento, le quantità relative di ciascun isotopo, espresse abitualmente in %, rappresentano le abbondanze isotopiche.
Gli isotopi che hanno una certa importanza negli studi idrogeologici sono:
Idrogeno 1H (idrogeno H;
2H (deuterio-D);
3H(Trizio-T)
- Ossigeno: 18O; 16O
- Carbonio: 12C; 13C; 14C
- Zolfo: 32S; 34S
- Azoto: 14N; 15N
Per separare isotopi diversi viene utilizzato lo spettrometro di massa, ma le misure assolute possono avere errori per questo vengono misurati i rapporti di abbondanza isotopici ( R ) riferiti ad uno standard di riferimento.
La composizione isotopica degli elementi viene comunemente espressa tramite l’unità delta.
La composizione isotopica degli elementi viene comunemente espressa tramite l’unità delta.
Il delta rappresenta la differenza in parti per mille del rapporto isotopico R nel campione rispetto allo stesso rapporto di uno standard di riferimento. Il suo valore dipende dunque dallo standard di riferimento adottato va misurato in millesimi ed è il valore numerico fornito dallo spettrometro di massa.
- Un valore positivo indica che l’isotopo pesante è arricchito nel campione rispetto allo standard;
- Un valore negativo indica che l’isotopo pesante è impoverito rispetto allo standard prescelto.
Il frazionamento isotopico è un numero base = 1 dove viene aggiunta la differenza dei delta delle due sostanze diviso mille; se d= 1,003 la differenza tra A e B corrisponde a tre millesimi (0,003).
tale Delta esprime approssimativamente il frazionamento isotopico in parti per mille, di un dato elemento contenuto in A e B.
Il fattore di arricchimento esprime la deviazione del fattore di frazionamento alfa da 1, ed è espresso in parti per mille:
tale Delta esprime approssimativamente il frazionamento isotopico in parti per mille, di un dato elemento contenuto in A e B.
Il fattore di arricchimento esprime la deviazione del fattore di frazionamento alfa da 1, ed è espresso in parti per mille:
Frazionamento Isotopico
Le abbondanze relative degli isotopi di uno stesso elemento non sono uguali nei composti naturali, questo è dovuto al fatto che esistono processi fisici e chimico-fisici capaci di operare con un certo grado di selettività nei confronti di vari isotopi di un elemento. La selettività isotopica è essenzialmente legata alla differenza di massa degli isotopi. Ci si aspetta che, a parità di altre condizioni, i frazionamenti isotopici siano tanto più grandi quanto maggiore è la differenza relativa di massa tra gli isotopi considerati.
per frazionamento isotopico di un dato elemento si intende la distribuzione delle varie specie isotopiche dell’elemento tra due o più fasi coesistenti. Si parlerà perciò di “arricchimento” (o di “impoverimento”) di un certo isotopo dell’elemento in questione in una fase relativamente alle altre.
IL fattore di Frazionamento (α) è definito dal rapporto fra i rapporti isotopici ( R ) di due composti chimici o di due fasi coesistenti A e B di un composto chimico che prendono parte ad un processo chimico-fisico:
Le abbondanze relative degli isotopi di uno stesso elemento non sono uguali nei composti naturali, questo è dovuto al fatto che esistono processi fisici e chimico-fisici capaci di operare con un certo grado di selettività nei confronti di vari isotopi di un elemento. La selettività isotopica è essenzialmente legata alla differenza di massa degli isotopi. Ci si aspetta che, a parità di altre condizioni, i frazionamenti isotopici siano tanto più grandi quanto maggiore è la differenza relativa di massa tra gli isotopi considerati.
per frazionamento isotopico di un dato elemento si intende la distribuzione delle varie specie isotopiche dell’elemento tra due o più fasi coesistenti. Si parlerà perciò di “arricchimento” (o di “impoverimento”) di un certo isotopo dell’elemento in questione in una fase relativamente alle altre.
IL fattore di Frazionamento (α) è definito dal rapporto fra i rapporti isotopici ( R ) di due composti chimici o di due fasi coesistenti A e B di un composto chimico che prendono parte ad un processo chimico-fisico:
Esempio fattore di frazionamento:
Viene definito rapporto isotopico o rapporto di abbondanza isotopica in un composto ( R ):
Il fattore di frazionamento α è importante alle basse temperature, mentre all’aumentare della temperatura è ritardato.
I principali processi chimico-fisici che possono determinare un frazionamento isotopico in natura sono:
I principali processi chimico-fisici che possono determinare un frazionamento isotopico in natura sono:
- Reazioni di scambio isotopico all’equilibrio;
- Processi cinetici, dovuti principalmente a differenze nella velocità di reazione
- Differenze nelle tensioni di vapore delle varie specie isotopiche nei liquidi